 MariaFerr
MariaFerrСпочноооооо посчитайтеее
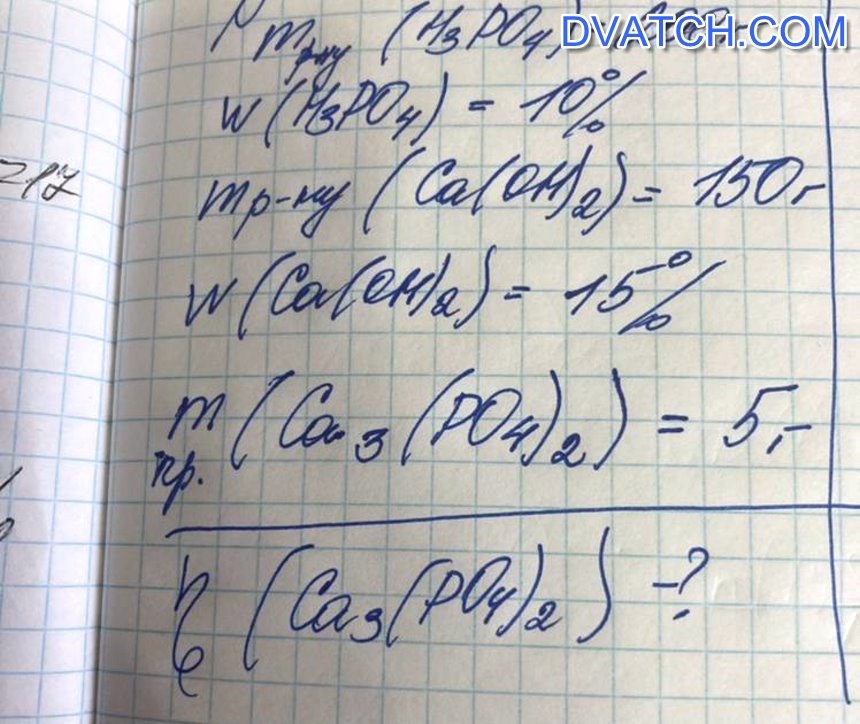
Дано:
m(р-ра H₃PO₄) = 200 гр
ω(H₃PO₄) = 10%
m(р-ра Ca(OH)₂) = 150 гр
ω(Ca(OH)₂) = 15%
m пр. (Ca₃(PO₄)₂) = 5 гр
---------------------------------------
Найти:
η(Ca₃(PO₄)₂) - ?
Решение:
1) Для начала мы запишем уравнение реакций:
2H₃PO₄ + 3Ca(OH)₂ → Ca₃(PO₄)₂ + 6H₂O
2) Далее находим массу чистого вещества у фосфорной кислоты и у гидроксида кальция:
m(H₃PO₄) = (m(р-ра H₃PO₄) × ω(H₃PO₄)) / 100% = (200 гр × 10%) / 100% = 200 гр × 0,1 = 20 гр
m(Ca(OH)₂) = (m(р-ра Ca(OH)₂) × ω(Ca(OH)₂)) / 100% = (150 гр × 15%) / 100% = 150 гр × 0,15 = 22,5 гр
3) Далее мы определим их количества вещества у фосфорной кислоты и гидроксида натрия, чтобы определить какое из них вещество будет в избытке а какой в недостатке:
M(H₃PO₄) = 1×3 + 31 + 16×4 = 3 + 31 + 64 = 98 гр/моль
M(Ca(OH)₂) = 40 + (16+1)×2 = 40 + 17×2 = 40 + 34 = 74 гр/моль
n(H₃PO₄) = m(H₃PO₄)/M(H₃PO₄) = 20 гр / 98 гр/моль ≈ 0,2 моль
n(Ca(OH)₂) = m(Ca(OH)₂)/M(Ca(OH)₂) = 22,5 гр / 74 гр/моль ≈ 0,3 моль Следовательно мы получаем что Ca(OH)₂ - в избытке, а H₃PO₄ - в недостатке.
4) Тогда мы по уравнению реакций, находим количества вещества у фосфата кальция , а потом его теоретическую массу мы находим:
n(H₃PO₄) : n(Ca₃(PO₄)₂) = 2 : 1 - по уравнению реакций, следовательно:
n(Ca₃(PO₄)₂) = 1/2 × n(H₃PO₄) = 1/2 × 0,2 моль = 0,1 моль
M(Ca₃(PO₄)₂) = 40×3 + (31 + 16×4)×2 = 120 + (31 + 64)×2 = 120 + 95×2 = 120 + 190 = 310 гр/моль
m теор. (Ca₃(PO₄)₂) = n(Ca₃(PO₄)₂) × M(Ca₃(PO₄)₂) = 0,1 моль × 310 гр = 31 гр
5) Теперь находим выход у фосфата кальция:
η(Ca₃(PO₄)₂) = m пр. (Ca₃(PO₄)₂) / m теор. (Ca₃(PO₄)₂) × 100% = 5 гр / 31 гр × 100% ≈ 0,1613 × 100% ≈ 16,13%
: η(Ca₃(PO₄)₂) = 16,13%
Решено от :
 hook up
hook up